
Una de las empresas de mayor trayectoria involucrada en la tecnología de la diabetes es Medtronic Diabetes, que ha tenido un camino retorcido en su cartera de productos a lo largo de los años.
La compañía ha sido líder en bombas de insulina desde hace décadas y fue la primera en lanzar un dispositivo combinado con un monitor continuo de glucosa (CGM). Como un poderoso líder de la industria farmacéutica, los pacientes tienden a tener una relación de amor y odio con esta empresa, apreciando sus ofertas pero no siempre su servicio al cliente o sus tácticas de marketing.
No importa cómo se mire, Medtronic Diabetes ayuda a liderar el camino en la tecnología de la diabetes, por lo que es importante saber qué está haciendo la empresa. A continuación, se incluye una descripción detallada de lo que ofrece Medtronic Diabetes en 2020 y más allá:
Herramientas actuales para la diabetes
A mediados de 2020, esto es lo que ofrece Medtronic Diabetes en cuanto a herramientas tecnológicas:
Minimed 670G (circuito cerrado híbrido)
El Minimed 670G fue el primero para nuestra comunidad de diabetes, con este circuito cerrado híbrido (HCL) temprano enganchando la aprobación de la Administración de Alimentos y Medicamentos (FDA) en septiembre de 2016.

“Circuito cerrado híbrido” en realidad solo significa que el sistema de administración de insulina está parcialmente automatizado, pero aún requiere cierto control por parte del usuario. La definición oficial de la FDA se vuelve un poco más técnica.
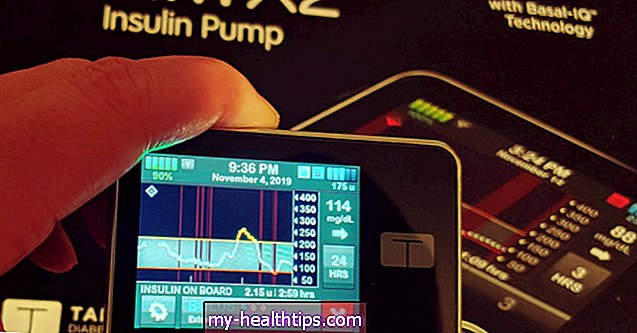
La forma en que funciona es que el sensor CGM lee los datos de glucosa cada 5 minutos, y el algoritmo de "circuito cerrado" integrado en la bomba utiliza esa información para aumentar o disminuir la administración de insulina basal (de fondo) para mantener los niveles de glucosa lo más cerca posible de un objetivo fijo de 120 mg / dL (para consternación de muchos usuarios, este nivel no se puede ajustar).
Los usuarios aún deben ingresar los recuentos de carbohidratos y las cantidades de bolo para cubrir las comidas y alertar al sistema antes de cualquier ejercicio. Tampoco proporciona bolos de corrección automática basados en MCG, pero sugiere cantidades de corrección cuando se ingresa un resultado de glucosa por punción digital.
El 670G se lanzó en 2017 con altas expectativas, pero al ser un "páncreas artificial" temprano y aún limitado con algunas limitaciones claras, no obtuvo una reacción positiva de las personas con diabetes tan fuerte como esperaba la compañía.
Consulte nuestra cobertura de noticias 670G y reseñas de productos para obtener más detalles.
Pluma de insulina inteligente: Companion's InPen
En agosto de 2020, Medtronic Diabetes anunció que estaba adquiriendo la puesta en marcha de Companion Medical y la pluma de insulina con Bluetooth, conocida como InPen. Esta es la única pluma de insulina reutilizable aprobada por la FDA que se conecta con una aplicación para rastrear datos y brinda a los usuarios recomendaciones de dosificación personalizadas para la insulina de acción corta (Humalog, Novolog, Fiasp).

Hasta ahora, las bombas de insulina eran el único método de administración de Medtronic que se ofrecía a los pacientes; pero ahora, al comprar su camino en el mercado de las plumas de insulina inteligentes, habrá una nueva opción para aquellos que elijan inyecciones en lugar de terapia con bomba.
Medtronic dice que no planea cambiar la capacidad del InPen para conectarse con CGM como el CGM implantable Dexcom y Eversense, y también planea incorporar conectividad para el CGM Guardian de Medtronic en el futuro.
Puede leer nuestra cobertura completa sobre la adquisición de InPen de Medtronic aquí.
Guardian Connect CGM
Guardian Connect es el nombre del dispositivo CGM independiente de Medtronic, que ha estado disponible desde marzo de 2018 y no necesita estar emparejado con una bomba de insulina para que funcione. The Guardian Connect fue el primer producto CGM nuevo e independiente de la compañía que se ofreció en una década.

A diferencia del sistema 670G que no ofrece ningún intercambio de datos ni monitoreo remoto, este CGM autónomo ofrece Bluetooth Low Energy incorporado para compartir datos directamente con un teléfono inteligente. Utiliza el mismo sensor Guardian 3 aprobado para su uso con el 670G y, en particular, evita la necesidad de un dispositivo receptor dedicado separado para ver los datos.
Esto no está libre de calibración, que es diferente de los productos CGM de la competencia (versiones Dexcom G5 y G6 y FreeStyle Libre) que no requieren confirmaciones por punción digital antes de cualquier tratamiento o dosis de insulina. También está aprobado para su uso a partir de los 14 años, lo que significa que los niños solo pueden obtener este producto si un médico está dispuesto a recetarlo "fuera de etiqueta".
Aplicación móvil Guardian Connect
En el momento del lanzamiento, esta aplicación gratuita solo estaba disponible para usuarios de iOS. Pero en mayo de 2020, Medtronic anunció la aprobación de la FDA para su versión de Android a partir del verano. Ahora también ofrece actualizaciones de algunas funciones de repetición y personalización bastante interesantes para rastrear y administrar el azúcar en la sangre, sobre las cuales puede leer aquí.
Aplicación móvil Sugar.IQ
Esta es una aplicación móvil separada a la que los usuarios de Guardian Connect CGM también tienen acceso exclusivo. Es la aplicación IBM Watson original que Medtronic adquirió y promocionó antes de lanzarla finalmente a un número limitado de clientes que utilizan su CGM independiente en 2017.
La aplicación utiliza análisis de IBM Watson para encontrar patrones en los datos de diabetes y ofrece información en tiempo real, procesable y personalizada, que incluye un gráfico circular que refleja los datos de tiempo en rango (TIR) y una llamada "Asistencia glucémica" para alimentos. info. Medtronic ha presentado datos científicos que muestran que las personas que utilizan el sistema Guardian Connect con la aplicación Sugar.IQ experimentaron un 4,1 por ciento más de TIR en comparación con el uso de Guardian Connect solo, lo que representa aproximadamente una hora extra por día. Además, aquellos que también utilizaron la función opcional de asistencia glucémica para revisar su respuesta a alimentos específicos aumentaron el TIR en un 4 por ciento adicional en comparación con aquellos que no utilizan esa función.

Productos futuros en desarrollo
Bajo un nuevo liderazgo desde octubre de 2019, la división de Diabetes de Medtronic reveló algunos detalles interesantes de su próxima cartera de tecnología de cara a la gran conferencia de la Asociación Estadounidense de Diabetes (ADA) en junio de 2020:
Lazo cerrado híbrido avanzado (780G)
Presentado por primera vez en torno a las sesiones científicas de la ADA en junio de 2019, el sistema de circuito cerrado híbrido avanzado (ACHL) de próxima generación 780G de la compañía tendrá el factor de forma básico de sus bombas de insulina modelo de la serie 6. Eso significa un aspecto vertical "moderno", en comparación con los modelos más antiguos con un diseño horizontal que se asemeja a los buscapersonas de los años 80.

Algunas características clave del 780G que hemos aprendido:
- utiliza un nuevo algoritmo que la compañía dice que es más preciso y confiable, desarrollado como resultado de la asociación con DreaMed Diabetes, con sede en Israel, anunciada en 2015.
- funciona con el sensor Zeus CGM de próxima generación, que tendrá solo 1 calibración el primer día y no requerirá punciones en los dedos después de eso.
- proporcionará un bolo de corrección automático cada 5 minutos para ayudar a mantener a los usuarios en un rango óptimo y para ajustar automáticamente las comidas omitidas.
- tiene un objetivo de glucosa ajustable entre 100 y 120 mg / dL (en comparación con el objetivo fijo del 670G a 120 mg / dL).
- ofrece diferentes tiempos de duración de la insulina, a diferencia de otros sistemas comerciales de circuito cerrado disponibles.
- ofrece Bluetooth integrado necesario para compartir datos y monitoreo remoto, así como actualizaciones de software remotas por aire para que los usuarios no tengan que comprar un dispositivo completamente nuevo cada vez que se lanzan nuevas funciones. (Actualmente, solo el Tandem t: slim X2 ofrece esa capacidad de actualización remota).
- Medtronic planea pedir a los reguladores que aprueben este nuevo sistema para adultos Y niños de tan solo 2 años desde el principio.
En las ADA Sci Sessions en junio de 2020, Medtronic publicó importantes datos de prueba fundamentales para este próximo sistema 780G, que muestra mejores resultados TIR e impresionantes marcas de satisfacción del usuario por la usabilidad del sistema.
Este sistema ahora cuenta con la aprobación de la marca CE en el extranjero, y la compañía se está preparando para presentar pronto el 780G ante la FDA aquí en los EE. UU.
770G conectado por Bluetooth
Medtronic recibió la aprobación de la FDA el 31 de agosto de 2020 para su 770G, que es el componente habilitado para BLE de su futuro dispositivo 770G. Esto se ve como una solución temporal entre el 670G existente y el 780G futuro, agregando conectividad Bluetooth para compartir datos y monitoreo remoto (algo que los dispositivos de la competencia como Dexcom han ofrecido durante años). En particular, está disponible para niños menores de 6 años y tan pequeños como 2.
Medtronic está lanzando el 770G primero como un dispositivo separado, antes del eventual lanzamiento del 780G con todas las funciones. La compañía señala que los clientes podrán actualizar fácilmente a 780G y funciones más nuevas de forma remota, en lugar de requerir una nueva compra de hardware (similar a lo que ofrece Tandem con su capacidad de actualización remota en t: slim X2).
Equipo de infusión de uso prolongado
Medtronic presentó recientemente datos sobre su equipo de infusión de 7 días, que se puede usar el doble de tiempo que los juegos actuales que están autorizados por un máximo de 3 días. Está en curso un ensayo fundamental en EE. UU. Y este nuevo equipo de infusión ya está aprobado en Europa.
En comunicados de prensa, Medtronic apunta a un "enfoque novedoso y patentado" que aborda la degradación de la insulina y la pérdida de conservantes, dos cosas que pueden provocar oclusiones (obstrucciones de insulina en los tubos de la bomba) y, por lo tanto, niveles más altos de azúcar en sangre. Además de mantener la estabilidad de la insulina durante los 7 días completos, también utilizará una nueva tecnología adhesiva para ayudar a garantizar que permanezca adherida al cuerpo durante todo ese tiempo de uso.
Los primeros datos clínicos muestran que las personas que usan este nuevo conjunto podrían ahorrar de 5 a 10 viales de insulina por año que actualmente se desperdician debido a la necesidad de cambiar el conjunto cada 3 días. Los cambios de conjuntos menos frecuentes también permitirían que otras ubicaciones de la piel descansen y se curen, señala Medtronic.
Sin embargo, se nos recuerda que los equipos de infusión se han descrito como el "talón de Aquiles" de la tecnología moderna de bombas de insulina porque tienden a tener muchas debilidades. Especialmente Medtronic no tiene el historial más exitoso en esta área. ¿Recuerda la tecnología BD FlowSmart que se lanzó como el conjunto Medtronic Pro? Eso no duró mucho, ya que los informes de cánulas torcidas llevaron a que Medtronic retirara el producto inicial del mercado. La compañía trabajó con BD para estudiar los problemas y planeó relanzar este equipo de infusión, pero finalmente BD descartó el concepto por completo.
Sensores CGM del futuro
Medtronic también está desarrollando sus sensores CGM de próxima generación, mejorando el juego desde sus sensores Enlite originales y la versión actual de Guardian 3 que viene junto con el Minimed 670G y el CGM independiente. La compañía ha insinuado futuros MCG durante años en presentaciones científicas, pero no se ha discutido mucho públicamente hasta mediados de 2020.

Por ahora, los dos nuevos modelos se conocen por nombres de proyectos internos que probablemente no serán las marcas definitivas:
- Sensor del Proyecto Zeus: aún tendría un uso de 7 días y el mismo diseño de concha, pero sería una clasificación “iCGM” (aprobada por la FDA para integrarse con otros dispositivos) y requeriría calibraciones por punción digital solo el primer día de uso.
- Project Synergy: un sensor / transmisor todo en uno que será completamente desechable y tendrá un nuevo aspecto. Con un factor de forma cuadrado más plano, un 50 por ciento más pequeño que el modelo actual, no requerirá ningún exceso de cinta para mantenerlo encendido y tendrá un proceso de inserción de tres pasos más simple que solo toma 10 segundos. No se sabe si tiene un tiempo de uso mayor de 7 días. Es probable que este sea al menos dentro de uno o dos años (~ 2022-23), ya que los estudios de investigación apenas están comenzando.

Lazo cerrado personalizado
Medtronic ya está trabajando en esta futura versión de su sistema de circuito cerrado que permitiría un control aún más personalizado a través de la interfaz del teléfono inteligente, con optimización de configuración automática, cobertura automática de carbohidratos opcional e IA (inteligencia artificial) que le permite adaptarse al comportamiento del paciente. Todo con una meta TIR del 85 por ciento. Parte de esto probablemente incluiría las adquisiciones de Medtronic de dos nuevas empresas, Nutrino Health y Klue, para el seguimiento de los gestos de las comidas y la ciencia de datos de nutrición.
Siempre es una cuestión de cuándo se enviará algo a la FDA, y mucho menos se aprobará realmente, pero considerando la designación innovadora de la FDA otorgada para este dispositivo en investigación en 2019, puede que no esté muy lejos.
Reclamación de dosificación (más cobertura de Medicare)
Medtronic ha tardado en buscar un estado "no adjunto" para sus sensores CGM que eliminaría el requisito de confirmaciones por punción digital y permitiría la cobertura de Medicare. Si bien todos los demás competidores de MCG se han enganchado a esta designación de la FDA, Medtronic se ha demorado en perseguirla.
Sin embargo, la compañía le dice a DiabetesMine que lo ha tenido en mente durante varios años y planea implementarlo para su sensor Guardian 3 y su sistema 780G en poco tiempo. Si lo aprueban los reguladores, permitiría que el sistema independiente Guardian 3 CGM de la empresa, así como los dispositivos con sensores aumentados, sean elegibles para la cobertura de Medicare.
¿Bomba de parche sin cámara?
Érase una vez, Medtronic Diabetes tenía la mira puesta en una bomba de parche que no incluiría los tubos tradicionales que tenían sus dispositivos. Los observadores de la industria recuerdan el plan de la compañía en 2008, solo unos pocos años después de que el Omnipod sin cámara llegara al mercado por primera vez, para desarrollar su propia bomba de parche desechable.
Medtronic Diabetes prácticamente descartó esa idea hace años, pero de vez en cuando recibe una mención y un interés renovado. A mediados de 2020, el Omnipod sigue siendo el único de su tipo, a pesar de muchos aspirantes a bombas de parche que han ido y venido y todavía están hablando de productos futuros.
Vía de interoperabilidad
Como parte de toda esta tecnología futura, Medtronic se está preparando para las pruebas fundamentales necesarias para obtener la codiciada clasificación de interoperabilidad “iCGM”. A mediados de 2020, Dexcom G6 tiene esta designación para funcionar con tecnología de circuito cerrado, mientras que FreeStyle Libre 2 tiene una versión limitada del estado iCGM, lo que significa que no se puede usar actualmente con dispositivos automáticos de administración de insulina.
En junio de 2019, Medtronic y Tidepool anunciaron que trabajarían en un futuro circuito cerrado interoperable, separado de los sistemas 780G / AHCL y de circuito cerrado personalizados antes mencionados. No se sabe qué tan lejos puede estar y qué características puede ofrecer.
Tecnología descontinuada
Finalmente, vimos el final de una era en cuanto a los modelos originales de bombas de insulina de Medtronic que parecían coloridos buscapersonas en 2018. Aún se usan ampliamente, pero ahora están oficialmente descontinuados y ya no están disponibles para comprar. Los suministros son cada vez más difíciles de encontrar a medida que avanza el tiempo.

En su apogeo, la Minimed 530 fue monumental porque hizo lo que ninguna otra bomba de insulina había hecho antes: suspendía automáticamente la administración de insulina si cruzaba un cierto umbral bajo de glucosa. Medtronic consiguió la aprobación de la FDA para esa función de suspensión baja en glucosa (LGS) o suspensión de umbral en septiembre de 2013 y permaneció disponible hasta octubre de 2018, cuando Medtronic la descontinuó y las bombas anteriores de la “serie 5” en favor de los dispositivos de la serie 6 más nuevos.
Irónicamente, muchos en la comunidad de innovación en diabetes #WeAreNotWaiting DIY (hágalo usted mismo) todavía están usando estos modelos de bomba de insulina más antiguos, ya que siguen siendo bastante confiables y, tápense los oídos, la FDA y los educadores en diabetes desconfían del uso de productos no aprobados. pueden ser pirateados.
A pesar de una advertencia de la FDA y de la preocupación de los principales medios de comunicación en 2019 acerca de que estos sistemas caseros no son ciberseguros debido a la tecnología obsoleta, permanecen en circulación.
El acceso a la diabetes es importante
El acceso y la asequibilidad son problemas críticos que existen como barreras a la tecnología para muchos dentro de la comunidad de la diabetes.
La cobertura de seguro juega un papel importante en eso, pero desafortunadamente Medtronic ha sido una compañía controvertida en ese frente en los últimos años.
En su impulso hacia la atención "basada en el valor" o "impulsada por los resultados", Medtronic firmó un acuerdo en 2016 con el gigante de seguros de salud United Health Care (UHC) que convirtió a las bombas de Medtronic en la "marca preferida" para los titulares de sus planes. En 2019 siguió un acuerdo similar para la última tecnología de Medtronic aprobada para niños.
Esta restricción de elección frotó a muchos en la Comunidad D de la manera incorrecta, por decirlo suavemente. Si bien UHC y Medtronic señalan que se pueden hacer excepciones en ciertos casos, la lucha continúa contra esta forma de cambio no médico que anula las preferencias del médico y el paciente por razones comerciales. Afortunadamente, UHC comenzó a ofrecer una opción el 1 de julio de 2020 cuando expandió los artículos cubiertos dentro de la marca para incluir la tecnología Tandem Diabetes junto con los productos de Medtronic.
Al final, todo se reduce a la simple realidad de que #DiabetesAccessMatters. Ninguna innovación de forma tiene impacto si la gente no puede conseguirla.
Si bien Medtronic ciertamente merece crédito por lo que ha logrado al traer nueva tecnología a la comunidad, les imploramos que también ayuden a fomentar la elección de pacientes y médicos.











.jpg)










