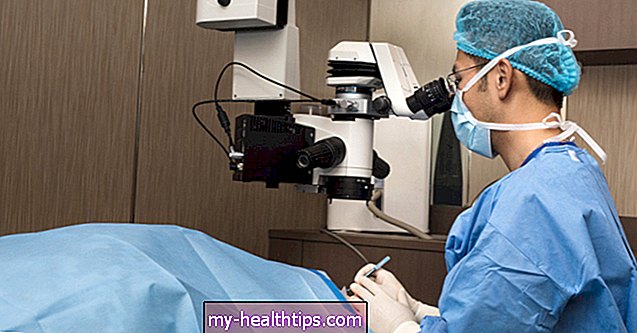
Una nueva generación de insulina inhalada se está acercando al mercado, ya que una compañía biofarmacéutica poco conocida se está preparando para la investigación clínica en etapa tardía y la presentación de la FDA, y acaba de contratar a un CEO experimentado para liderar los esfuerzos de comercialización.
Quizás recuerde Dance Biopharm, la startup del área de San Francisco que entró en escena aproximadamente en 2010, después de que la insulina inhalada Exubera estilo bong fallida de Pfizer fuera retirada del mercado y cuando Afrezza de MannKind todavía estaba en desarrollo. Esta startup ha estado trabajando para crear un tipo completamente nuevo de insulina inhalada durante casi una década.
La compañía ahora está en los titulares con la reciente contratación de la ex ejecutiva de Sanofi Anne Whitaker, quien está bastante familiarizada con el universo de la insulina inhalada y el aspecto comercial de llevar nuevos medicamentos al mercado. Tiene su sede en Carolina del Norte, donde Dance Biopharm se está preparando para trasladar su sede en los próximos meses. Se quedarán en la costa oeste para investigar, pero los ejecutivos estarán en la costa este mientras Dance también se prepara para abrir oficinas en China e Inglaterra en poco tiempo.
“Hemos estado fuera del radar, se podría decir trabajando en modo sigiloso. Pero cuando miras el progreso realizado, es notable. Todas esas cosas se unen ... ahora es el momento de llevar esto adelante ”, dice Whitaker sobre su novedoso producto actualmente denominado Dance 501 (el nombre de trabajo interno).
En una conversación telefónica reciente, Whitaker nos contó por qué se unió al equipo de Dance y qué podemos esperar en los próximos años. Pero primero, echemos un vistazo a esta nueva insulina inhalada y las ventajas que ofrece a los pacientes.
Sizing Up Dance 501, también conocida como insulina inhalada 3.0
La FDA revisará y aprobará cualquier nombre de marca de producto propuesto para esta nueva insulina inhalada, a la que algunos se refieren como Generación 3.0. A continuación, se muestran las propiedades de lo que todavía se conoce como Dance 501:

Soft Mist: a diferencia de la insulina Afrezza de MannKind, que es un polvo blanco inhalable, Dance 501 es una formulación en neblina, es decir, una insulina recombinante ultraconcentrada que requiere solo unas pocas gotas que se vaporizan en forma de neblina a medida que la inhala profundamente en los pulmones a través de un pequeño dispositivo de mano.
Pura: a diferencia de otras insulinas, este producto no contiene conservantes, lo cual es importante para el 1-2% de las personas con discapacidad que en realidad tienen alergia a la insulina, lo que crea problemas que van desde erupciones en el sitio de la insulina hasta shock anafiláctico. Viene en forma líquida en una botella pequeña, que se usa para llenar el dispositivo de mano justo antes de cada dosis.
Inhalador de mano: pequeño y fácil de usar, tiene aproximadamente el tamaño de un buscapersonas de la vieja escuela que cabe en el bolsillo de un pantalón. Esto es bastante diferente a los primeros prototipos que vimos; en diciembre de 2017, la compañía se asoció con el diseñador industrial Phillips-Medisize para una versión renovada. El resultado es un inhalador electrónico que utiliza una tecnología patentada de malla vibratoria diseñada para producir partículas de insulina líquida de tamaño constante en forma de una niebla suave. (Dato curioso: ¡hay 120.000 vibraciones en un segundo!). El dispositivo se activa con la respiración y solo se necesitan unas pocas respiraciones para inhalar la niebla de insulina Dance 501, con una luz verde que indica que está respirando la niebla de manera adecuada antes de que una luz azul en el dispositivo parpadee para indicar que ha terminado. Whitaker dice que recientemente enviaron a la FDA sus recomendaciones de diseño para el dispositivo inicial y esperan escuchar comentarios regulatorios a principios de noviembre.
Dispositivo inhalador de próxima generación: mientras que la primera generación usa un par de baterías AA, Whitaker dice que es probable que eso cambie tan pronto como seis meses después del lanzamiento con un dispositivo recargable de segunda generación. Eso reducirá el tamaño y el peso del dispositivo en un 50%, para que se parezca más a un tubo de lápiz labial Chanel.
Acción más rápida: Whitaker dice que Dance 501 actúa más rápido que las insulinas tradicionales (Humalog, específicamente) y mejora la insulina inhalada de Afrezza, porque la acción de la insulina alcanza su punto máximo con la misma rapidez pero tiene una "cola más larga" que imita más de cerca la reacción natural del cuerpo sin una necesidad de dosis de seguimiento. Los estudios de fase II muestran pocas hipoglucemias y muy poca tos de las personas que usan esta niebla de insulina inhalada, que llega de forma más natural a los pulmones sin irritar la garganta.

Seguimiento de datos y conectividad: dado que el dispositivo inhalador es básicamente una pequeña computadora, registra datos de uso de insulina como cantidades de dosis, cuándo se toma, tasa de inhalación, cantidades de dosis de insulina y cuánta niebla entra realmente en los pulmones según la profundidad de la respiración. Dance también planea lanzar una aplicación móvil para el teléfono inteligente que contiene esos mismos datos, para que los pacientes la vean junto con los proveedores de atención médica y, finalmente, se conecten con otros dispositivos D como CGM y plataformas de datos. Todo eso es único, ya que otros dispositivos de insulina inhalada hasta la fecha no han ofrecido rastreo ni conectividad de dispositivos.
Tiempo de I + D: por muy emocionante que sea Dance 501, la paciencia será una virtud aquí ... hablaremos al menos dentro de unos años, si no más. Dance ha publicado investigaciones clínicas tempranas en los últimos años, y eso continúa con los ensayos de Fase II en curso hasta lo que se espera que sea a mediados de 2019. A partir de ahí, esperan comenzar los ensayos de fase III en etapa tardía en 2020 y probablemente llegar al punto de presentación reglamentaria para fines de ese año. Por supuesto, la financiación es clave para todo esto, por lo que el tiempo puede variar según eso, así como lo que muestre la investigación y lo que finalmente digan los reguladores.
Precios: Whitaker también dice que todavía están estudiando el precio y el costo. No cree que Dance 501 sea "un valor atípico para las insulinas existentes en la actualidad", pero al globalizarse en lugar de solo en EE. UU., Eso ayudará a compensar los precios para los pacientes. Por supuesto, también planean trabajar con los pagadores antes de pasar al mercado.
Formulación líquida, también: El hecho de que Dance esté desarrollando esta forma de niebla de insulina inhalada no significa que no estén buscando una versión líquida para usar en un vial / jeringa, bolígrafo o bomba de insulina, similar a la marcas tradicionales en el mercado ahora, nos dice Whitaker.
Muy emocionante, pero por supuesto, los pacientes impacientes no podemos evitar preguntarnos: ¿Qué diablos ha tardado tanto en llegar a este punto y por qué todavía estamos a años de ver este producto de Dance?
Hay muchas partes móviles, explicadas muy bien en nuestra charla con Whitaker.
Detrás de escena con la directora ejecutiva de Dance Biopharm, Anne Whitaker

Whitaker tiene un currículum bastante bueno con más de un cuarto de siglo en las industrias farmacéutica, de ciencias de la vida y biotecnología, desde diabetes hasta oncología, cardiovascular, respiratoria y gastroenterología. Su experiencia incluye la presidenta y directora ejecutiva de KNOW Bio, Novoclem Pharmaceuticals, Inc. y Synta Pharmaceuticals, Inc. Lo más notable para nuestra D-Community, por supuesto, es su tiempo como presidenta de la región de América del Norte para Sanofi de 2011 a 2014, donde tenía la responsabilidad de todas las unidades comerciales de productos farmacéuticos, dispositivos y atención médica para el consumidor.
Durante esos tres años en Sanofi, Whitaker dice que la compañía trató de impulsar el uso de insulina con Lantus y se centró principalmente en tratar de que las PWD (personas con diabetes) recogieran sus recetas y usaran los medicamentos de manera adecuada. Ella dice que solo el 30% de sus pacientes T2 previamente no dependientes de insulina obtuvieron sus recetas debido al miedo y la confusión en torno al uso de insulina.
Sabía de Dance hace mucho tiempo durante su tiempo en Sanofi, e hizo una revisión completa de la compañía mientras el gigante farmacéutico se preparaba para ingresar al mercado de la insulina inhalada. Whitaker señala que Sanofi eligió asociarse con MannKind (fabricantes de Afrezza) debido a una “oportunidad inmediata” de llevar un producto al mercado más rápidamente que Dance. Esa fue vista como una excelente manera de alejar el uso de insulina de los inyectables, explica. Pero ella dice que la compañía no comercializó Afrezza de la forma en que debería haberlo hecho para que tuviera una presencia más fuerte para las personas con discapacidad, y terminó abandonando Sanofi en 2014.
El ex ejecutivo de Sanofi dice: "Estaba frustrado"
"No se puede lanzar un producto en una posición terciaria", dijo. “Sinceramente, me sentí frustrado al verlo desde lejos. Porque vi el potencial de la insulina inhalada. Es por eso que Dance quería contratar a alguien con esta experiencia de comercialización ... tenemos que empezar a centrarnos en la preparación comercial ahora. Estamos comenzando ese proceso ahora y toda la comunidad diabética estará escuchando más de nosotros mientras nos preparamos para el lanzamiento ".
Whitaker agrega que creció en Alabama en el medio del "cinturón de diabetes" del sur, y debido a que también tiene una tía y un tío que viven con diabetes tipo 2 y su suegro tiene diabetes, ha observado la montaña rusa emocional que las PCD sobrellevar y cómo los médicos utilizan con demasiada frecuencia la insulina como una amenaza para las personas con diabetes tipo 2.
“Espero poder cambiar eso e impulsar el uso temprano de insulina antes de que atraviesen este continuo declive en su camino hacia la diabetes”, dice Whitaker. “Dance tiene un producto con Dance 501 que puede ofrecer otra opción. Ciertamente no es para reemplazar las bombas o la insulina basal, pero tiene un lugar antes en el paradigma del tratamiento ".
Por supuesto, Whitaker sabe que es una batalla cuesta arriba tratar de convencer a los inversores y a otras personas sobre el potencial de la insulina inhalada. Pero ella cree que lo que ha cambiado en la última década, luego del fracaso de Exubera, el lanzamiento y relanzamiento de Afrezza por MannKind y la evolución general de la tecnología y la nebulización en todo el mundo, ha preparado el escenario para Dance 501 de una manera que antes no era posible. .
El fundador de Dance, John Patton, fue cofundador y director científico de Nektar Therapeutics, que proporcionó la base científica para Exubera, y ahora sigue siendo parte de Dance con un puesto en la junta directiva. Otra ejecutiva con la que hablamos en 2011 es Samantha Miller, quien sigue siendo consultora estratégica de la empresa mientras se prepara para la comercialización.
Curiosamente, Whitaker dice que Dance Biopharm había planeado solicitar una OPI (oferta pública inicial) a fines de 2015, pero cuando Sanofi abandonó Afrezza de MannKind, ese plan cambió. En cambio, la compañía ha seguido adelante con los estudios clínicos y ha revisado su dispositivo para que sea más elegante y sofisticado.
Un ambiente maduro para inhalables
Los tiempos ciertamente han cambiado, lo que le da a Dance razones para creer que la gente está más abierta a la idea de los inhalables.
En estos días, los cigarrillos electrónicos y los vaporizadores se han vuelto comunes en todo el mundo, y Whitaker señala que la nebulización médica está explotando y se está volviendo más aceptada a nivel mundial. Ella cita cómo el 8% del mercado de medicamentos de EE. UU. Usa nebulizadores de mano para medicamentos esteroides, en comparación con el 12% en Europa y el 20% en China.
“El potencial para salir al mercado y comercializar Dance 501 con éxito, está ahí. El momento es el adecuado para Dance ”, dice Whitaker.
El costo de fabricación es ciertamente una preocupación en la mente de Whitaker, ya que es muy consciente de cuánto cuestan fabricar Exubera y Afrezza y llegar al mercado: más de mil millones de dólares (!) Pero ella dice que Dance puede esperar gastar solo una fracción de esos costos, ya que están trabajando con el mayor fabricante de insulina de Asia para tener plantas inspeccionadas por la FDA para la fabricación de Dance 501 para los EE. UU. en el extranjero.
"También somos afortunados de estar sobre los hombros de la insulina inhalada que vino antes que nosotros, porque ahora hay una gran cantidad de datos sobre la seguridad, la eficacia y el uso por parte de los pacientes", agrega.
Whitaker también agrega que los equipos de investigación y fabricación de la compañía permanecerán en el área de San Francisco, mientras que la sede comercial de Dance Biopharm se mudará a Research Triangle Park en Carolina del Norte dentro de los próximos 6 a 9 meses, y hasta entonces estarán operando. de forma remota. También planean abrir una oficina europea y una en China, dijo.
¿La insulina inhalada está ganando terreno?
Seguimos siendo cautelosamente optimistas sobre el potencial de este nuevo producto. Tome Afrezza de MannKind como ejemplo: los dos aquí en el 'Mío úsalo y ámalo. Pero el hecho es que MannKind ha tenido problemas y sus números de prescripción siguen siendo bajos, y muchos médicos todavía dudan en general sobre la formulación en polvo que ha estado en el mercado desde 2015. El mercado de la insulina es competitivo y voluble, y nada está garantizado (excepto el hecho que nosotros, las personas con discapacidad con DT1, no podemos prescindir de él).
Aún así, con todo eso en mente, tenemos la esperanza de que Dance llegue al mercado y pueda tener éxito donde Exubera fracasó y donde MannKind está luchando por afianzarse.
ACTUALIZACIÓN: En septiembre de 2019, la compañía se rebautizó como Aerami Therapeutics.


.jpg)
















.jpg)